Tiazole
| Substància química | tipus d'entitat química  |
|---|---|
| Massa molecular | 84,999 Da  |
| Estructura química | |
| Fórmula química | C₃H₃NS  |
 | |
| SMILES canònic | Model 2D C1=CSC=N1  |
| Identificador InChI | Model 3D  |
| Propietat | |
| Punt de fusió | −33 °C  |
El tiazole, o 1,3-tiazole, és un compost heterocíclic que conté sofre i nitrogen; el terme "tiazole" també es refereix a una gran família de derivats. El tiazole és un líquid de color groc pàl·lid amb una olor similar a la piridina i té per fórmula molecular C₃H₃NS.[1] L'anell de tiazole destaca per ser un component de la vitamina tiamina (B1).
Estructura molecular i electrònica
Els tiazoles són membres del grup de composts heterocíclics anomenat azoles, que inclouen imidazoles i oxazoles. El tiazole també pot ser considerat com un grup funcional.
L'anell de tiazole és pla, donat que els tiazoles són compostos aromàtics, i es caracteritzen per una deslocalització d'electrons pi més gran que els oxazoles corresponents. 
Síntesi
Hi ha diversos mètodes de laboratori per a la síntesi orgànica de tiazoles:
- La síntesi de tiazole de Hantzsch (1889): és una reacció entre halocetones i tioamides.[2] Un altre exemple,[3] es mostra a sota:
- En una adaptació de la síntesi de Robinson-Gabriel, 2-acilaminocetones reaccionen amb pentasulfur de fòsfor.
- En la síntesi Cook-Heilbron, una α-aminonitril reacciona amb sulfur de carboni.

- Certs tiazoles es fan per la reacció de Herz.
Reactivitat general
La reactivitat del tiazole es pot resumir com:
- La desprotonació en C2.
- El 2-(trimetilsilil)tiazol[4] (amb un grup trimetilsilil en la posició 2) reacciona amb una varietat d'electròfils, com els aldehíds, halurs d'acil, i cetena.
- La substitució electròfila aromàtica en C5 requereix grups d'activació com el grup metil en aquesta bromació:

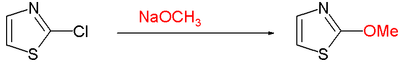
- La substitució nucleòfila aromàtica en C2 sovint requereix grups electròfugs o grups sortints com el clor de l'exemple:
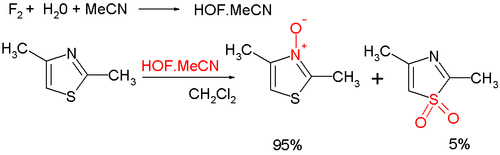
- L'oxidació orgànica del nitrogen dona el N-òxid de tiazole.[5]
- Els tiazoles poden reaccionar en reaccions de cicloaddició[6]

Usos
El tiazole es fa servir com material de partida per a la producció de fungicides, productes farmacèutics i colorants. Per exemple, formen part de la vitamina B1, la penicil·lina, l'epotilona (nova classe de fàrmacs antitumorals), luciferina, clometiazol i altres.
Referències

- ↑ The Chemistry of Heterocycles : Structure, Reactions, Syntheses, and Applications Theophil Eicher, Siegfried Hauptmann ISBN 3-527-30720-6
- ↑ Schwarz, G. (1945). "2,4-Dimethylthiazole". Org. Synth. 25: 35; Coll. Vol. 3: 332.
- ↑ Alajarín, M.; Cabrera, J.; Pastor, A.; Sánchez-Andrada, P.; Bautista, D. «On the [2+2] Cycloaddition of 2-Aminothiazoles and Dimethyl Acetylenedicarboxylate. Experimental and Computational Evidence of a Thermal Disrotatory Ring Opening of Fused Cyclobutenes». J. Org. Chem., 71, 14, 2006, pàg. 5328–5339. DOI: 10.1021/jo060664c. PMID: 16808523.
- ↑ Alessandro Dondoni and Pedro Merino (1998). "Diastereoselective Homologation of D-(R)-Glyceraldehyde Acetonide using 2-(Trimethylsilyl)thiazole". Org. Synth.; Coll. Vol. 9: 952.
- ↑ Elizabeta Amir and Shlomo Rozen «Easy access to the family of thiazole N-oxides using HOF·CH3CN». Chemical Communications, 2006, 21, 2006, pàg. 2262–2264. DOI: 10.1039/b602594c. PMID: 16718323.
- ↑ Mateo Alajarín, José Cabrera, Aurelia Pastor, Pilar Sánchez-Andrada, and Delia Bautista «On the [2+2] Cycloaddition of 2-Aminothiazoles and Dimethyl Acetylenedicarboxylate. Experimental and Computational Evidence of a Thermal Disrotatory Ring Opening of Fused Cyclobutenes». J. Org. Chem., 71, 14, 2006, pàg. 5328–5339. DOI: 10.1021/jo060664c. PMID: 16808523.

